Anticorps monoclonaux et systèmes à usage unique dans les bioprocédés
Qu'est-ce qu'un anticorps monoclonal ?
Les anticorps monoclonaux (AcM) sont un type de protéine utilisé dans le traitement de diverses maladies. Ils sont fabriqués par des cellules immunitaires identiques qui sont toutes des clones d'une seule cellule mère, d'où le nom "monoclonal".
Les AcM agissent en se fixant sur des cibles particulières appelées antigènes (souvent des récepteurs distincts présents à la surface des cellules), avec une affinité et une spécificité très élevées, de la même manière que les anticorps du système immunitaire.
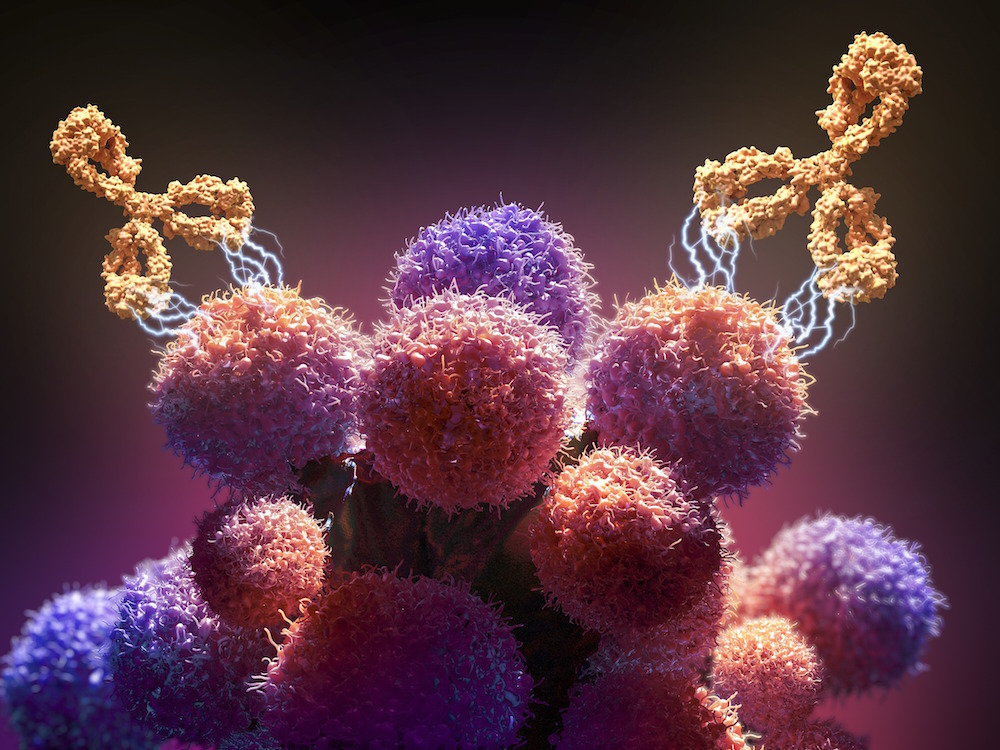
Cette liaison peut avoir divers effets, en fonction de la cible et de l'AcM en question. Par exemple, elle peut conduire à l'élimination de la tumeur par l'inhibition de fonctions essentielles des cellules malignes telles que la dimérisation ou les processus de propagation de la cascade de signaux. En outre, les AcM peuvent également se lier à des enzymes cibles pour faciliter leur élimination ou même être utilisés pour délivrer des molécules thérapeutiques directement aux cellules cancéreuses lorsqu'ils sont conjugués à des médicaments.
Les AcM sont produits par la technologie des hybridomes, une méthode dans laquelle les cellules B, un type de globules blancs qui produisent des anticorps, sont prélevées (généralement chez la souris ou d'autres mammifères) et fusionnées avec des cellules cancéreuses immortelles appelées myélomes, ce qui conduit à la création de cellules hybrides appelées hybridomes. Ces hybridomes peuvent être cultivés de la même manière que des lignées cellulaires ordinaires, ce qui permet de développer des lignées cellulaires génétiquement identiques capables de produire un seul anticorps spécifique.
Avantages des anticorps monoclonaux
Le principal avantage des anticorps monoclonaux est leur spécificité, leur sélectivité et leur affinité élevées. Cela leur permet de distinguer des récepteurs particuliers et de n'affecter que les cellules malignes (dans les cas de cancer) ou les bactéries infectieuses. Les cellules saines et les bactéries bénéfiques ne sont donc pas touchées, ce qui réduit la toxicité du traitement et les effets secondaires, augmentant ainsi la sécurité de la thérapie et le bien-être général du patient.
Une autre raison du succès des thérapies basées sur les AcM est qu'ils peuvent être modifiés pour moduler leurs propriétés. Comme tous les anticorps, les AcM sont constitués de trois segments : deux régions identiques de liaison à l'antigène, appelées Fabs, et une région singulière hautement conservée, appelée Fragment cristallisable (Fc), qui influe sur la réponse immunitaire des molécules.
En modifiant les régions Fabs, il devient possible d'améliorer l'affinité et la stabilité, et même de permettre la liaison à diverses cibles thérapeutiques. Parallèlement, les ajustements de la région Fc permettent d'affiner l'activité de la molécule, ce qui favorise la création d'approches immunothérapeutiques innovantes.
Enfin, les AcM sont également devenus une thérapie précieuse pour le traitement des infections et des maladies virales en se liant aux antigènes viraux et en les neutralisant ou en stimulant le système immunitaire du patient pour qu'il les élimine.
Production et applications des AcM par biotraitement.
Aujourd'hui, les AcM constituent l'une des classes de produits biothérapeutiques qui connaissent la croissance la plus rapide et dominent l'industrie depuis près de 30 ans.
En utilisant des cellules hôtes génétiquement modifiées, telles que les cellules ovariennes de hamster chinois (CHO), les AcM peuvent être produits en grandes quantités dans des bioréacteurs, ce qui permet une production efficace et rentable de médicaments vitaux pour le traitement de diverses maladies, notamment le cancer, l'inflammation et les troubles auto-immuns.
Outre leur utilisation comme molécules thérapeutiques, les AcM peuvent également être produits pour servir de réactifs et d'outils dans la purification et l'analyse d'autres protéines. Ils peuvent isoler des protéines spécifiques à partir de mélanges complexes, tels que des lysats sanguins ou cellulaires, en se liant à la protéine cible et en l'extrayant ensuite à l'aide de techniques telles que la purification par billes magnétiques ou la cytométrie de flux. De même, ils constituent des outils très précieux pour le diagnostic, la détection et la prévention d'un large éventail de maladies.
Avantages de l'utilisation de systèmes à usage unique (SUS) dans le domaine des bioprocédés
Les composants de haute qualité de Venair pour une mise en œuvre sans faille
Ces dernières années, l'utilisation de systèmes à usage unique (SUS) s'est généralisée dans l'industrie des bioprocédés, principalement en raison de leur facilité d'utilisation, de leur rentabilité, de la réduction des étapes de nettoyage et de validation et de l'atténuation du risque de contamination des procédés.

La flexibilité des SUS permet également d'augmenter ou de réduire facilement l'échelle des processus. Les tubes en silicone, les poches en polyéthylène et d'autres composants à usage unique sont importants pour la mise en œuvre de systèmes à usage unique dans la production d'AcM et d'autres applications de bioprocédés.
Venair propose une variété de tubes en silicone, de poches en polyéthylène et d'autres composants à usage unique qui conviennent parfaitement à l'industrie des bioprocédés et peuvent aider les entreprises à mettre en œuvre des systèmes à usage unique dans leurs processus de fabrication.
Conclusions
Dans l'ensemble, les AcM constituent un outil puissant dans la lutte contre les maladies et sont de plus en plus utilisés dans l'industrie des bioprocédés pour la production de protéines thérapeutiques et comme réactifs pour la purification et l'analyse. Avec l'avènement des systèmes à usage unique et les progrès de l'ingénierie, la production d'AcM est devenue plus efficace et plus rentable, rendant ces médicaments vitaux plus largement disponibles pour les patients qui en ont besoin.






